生体内輸送蛋白質を利用したドラッグデリバリーシステムの開発
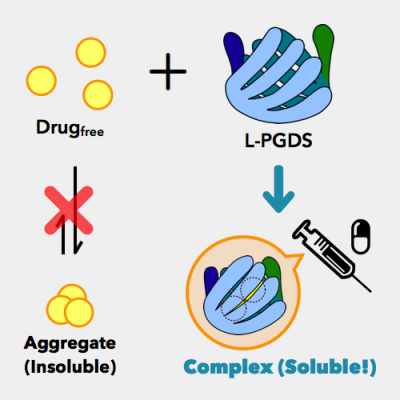
創薬において,新規に開発される薬剤候補化合物の多くは,水に溶けにくい,いわゆる難水溶性化合物である。化学修飾によりこれらの化合物の溶解度を上昇させることは可能であるが,薬剤活性を減じてしまう場合が多く,結果としてこのような難水溶性化合物は,薬剤候補から除外されてしまう。
当研究室では,生体内に存在する脂溶性低分子輸送蛋白質 (リポカリン蛋白質質) の一つであるリポカリン型プロスタグランジンD合成酵素 (L-PGDS,Fig. 1) を利用して,難水溶性薬剤を可溶化し,癌などの組織を狙い撃つ標的指向性を有するドラッグデリバリーシステム (DDS,Fig. 2) の開発を行っている。本DDSにより,これまでに開発段階で除外された難水溶性薬剤に再び脚光を当てることができる。
L-PGDSは,哺乳動物の中枢神経系に高発現し,PGD2合成酵素,活性酸素スカベンジャー [1],および分泌型の脂溶性低分子輸送蛋白質 [2] として機能するユニークな多機能蛋白質である。さらに我々は,L-PGDSがくも膜下出血誘導性の血管攣縮,および神経細胞死に関与しているビリベルジンのスカベンジャーとしても働いていることを報告している [3]。
本DDSの開発に先駆けて,当研究室ではNMR法やX線小角散乱法 (SPring-8) により,マウスやヒト由来L-PGDSの構造解析,および脂溶性低分子複合体の構造解析を行ってきた [4]。また,トリプトファン蛍光消光測定,誘起円偏光二色性測定,および等温滴定型熱量測定を用いて,L-PGDSと脂溶性低分子との相互作用解析も行っている [5, 6]。また, L-PGDSベースのDDSに適した薬物分子の探索に, ドッキングシュミレーションが有用であることも報告している[7]。
そして現在までに,疾患モデルマウスと難水溶性薬剤/L-PGDS複合体を用いた薬理実験において,L-PGDSを用いたDDSが経口投与,および静脈内投与の両投与法において有用であることを明らかにした [8]。また最近では,本DDSの難水溶性抗癌剤およびその誘導体への適応 [9, 10],および難水溶性薬剤/L-PGDS複合体の経口固形製剤化技術の開発 [11, 12] について報告している。
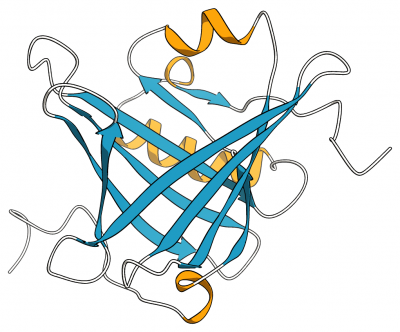
Figure 1. マウス由来L-PGDSのNMR溶液構造 (PDB code: 2RQ0)
8本のアンチパラレルβ-ストランド (β-バレル構造,青色) と1本の長いα-ヘリックス (橙色) からなる。
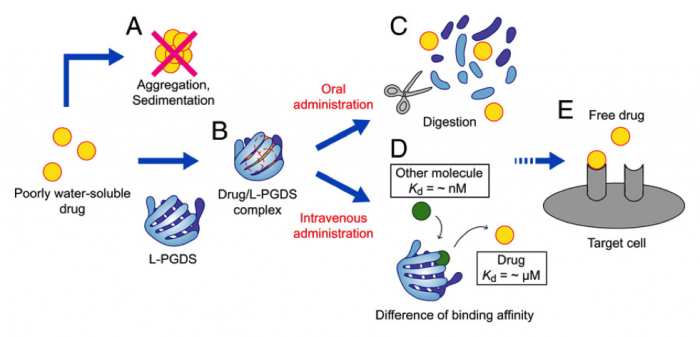
Figure 2. L-PGDSを用いたDDSの概念図
(A) 難水溶性薬剤は,水溶液中では凝集沈殿するため,直接投与することが困難である。(B) ここにL-PGDSを加えると,薬剤/L-PGDS複合体を形成することにより,薬剤の溶液中濃度が上昇し,生体内に効果的に輸送することができる。(C) 薬剤/L-PGDS複合体の経口投与では,胃内環境においてペプシン消化耐性を有するL-PGDSは,薬剤を保持したまま胃を通過した後に小腸まで到達し,小腸内のプロテアーゼによって速やかに消化される。小腸内で放出された難水溶性薬剤は,腸管から容易に吸収される。(D) 一方,薬剤/L-PGDS複合体の静脈内投与では,L-PGDSとより強く結合する血中のリガンドによって薬剤分子が追い出され,血中薬剤濃度が上昇する。(E) 結果的に,薬剤分子は標的細胞の受容体へ到達する。
- Fukuhara, A.; et al. Biochem. J. 443, 75–84 (2012).
- Inui, T.; et al. J. Biol. Chem. 278, 2845–2852 (2003).
- Inui, T.; et al. J. Cereb. Blood Flow Metab 34, 1558–1567 (2014).
- Miyamoto, Y.; et al. J. Struct. Biol. 169, 209–218 (2010).
- Kume, S.; et al. Biochem. J. 446, 279–289 (2012).
- Kume, S.; Lee, Y. H.; et al. FEBS Lett. 588, 962–969 (2014).
- Teraoka, Y.; et al. Mol. Pharm. 14, 3558–3567 (2017).
- Fukuhara, A.; et al. J. Control. Release 159, 143–150 (2012).
- Nakatsuji, M.; et al. PLOS ONE 10, e0142206 (2015).
- Doi, H.; et al. ChemMedChem. 12, 1715–1722 (2017).
- Mizoguchi, M.; et al. Eur. J. Pharm. Sci. 74, 77–85 (2015).
- Mizoguchi, M.; et al. J. Pharm. Sci. S0022-3549(15)00176-8 (2016).